

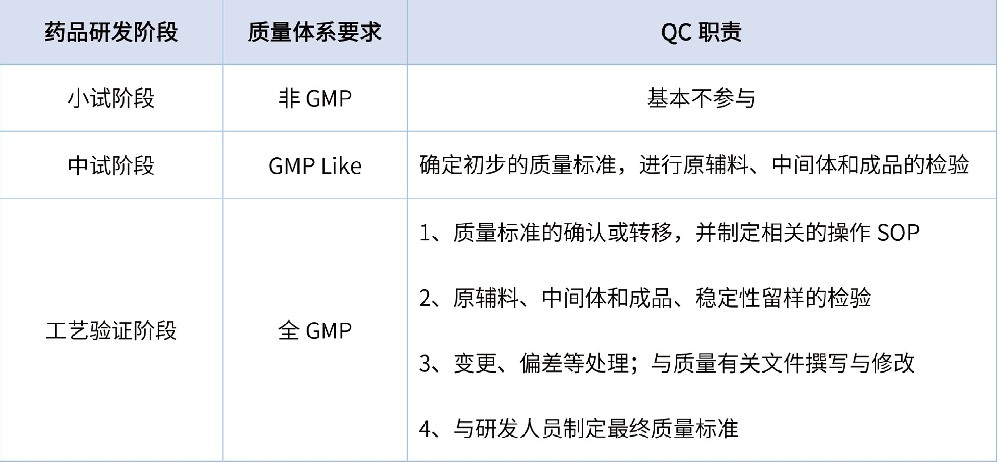
按照最新版《药品管理法》(2020版)要求,在药品全生命周期中需执行四个最严,即“最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责”。为保证药品的安全性和有效性,药品研发作为药品生命周期的源头,需在遵循《药品管理法》的前提下执行好《药品注册管理办法》法规要求。药品研发按创新药、改良型新药、仿制药进
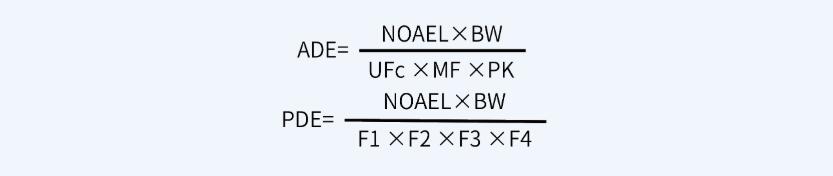
药品生产后必须对其生产设备采取一定的程序进行清洗,防止药物成分残留到下一批产品中,形成交叉污染,从而影响下一批产品的质量及安全性。清洁验证是证实清洗程序合理性的必要技术手段。WHO、EU、ICH、FDA及我国药品GMP均对药品生产清洁验证提出了相关要求:1)使用同一生

色谱柱的柱效能是评价色谱性能的一项重要指标,混合物能否在色谱柱中得到分离,除取决于选择合适的固定相外,还与色谱操作条件及色谱柱的装填状况等因素有关。在一定的色谱操作条件下,色谱柱的柱效可用理论塔板数或理论塔板高度来衡量。一般说来塔板数愈多,或塔板高度愈小,色谱柱的分离效能愈好。如何对柱效进行评价实验
一、元素的分布1.地球在不同深度的結构 地球除地壳部分可以直接研究外,它的内部秸构是依靠地震波在不同密度各层间的反射作用而得出结论的。地球按课度分层,共有五个层,称为界, 如图28-13所示,各界的成分见表28-13。除在图中标明的各界深度外,II硅酸盐外壳厚120公里。一般所谓地壳,大約指20公里的厚度而言,
导读:近期CDE官网更新了:仿制药质量和疗效一致性评价百问百答(第3期),其中包括「杂质研究+溶出曲线对比」新规问:口服固体制剂一致性评价杂质研究需要注意哪些问题?答:口服固体一致性评价品种均为已上市品种,杂质研究中可以参考的文献资料较多,但是杂质研究不全面或过度研究,均可能给研发和审评带来不必要的负担,
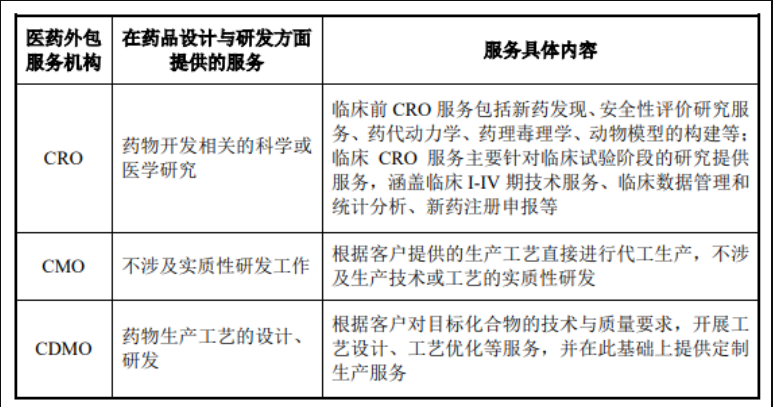
CDMO企业与CMO、CRO企业在药品设计与研发方面的差异:近年来,全球医药行业的竞争日趋激烈,制药产业链中的分工日益细化,医药行业的专业化外包已成为制药企业的重要战略选择。随着医药外包服务机构专业化程度的不断提高, 医药外包服务的内容逐渐涵盖了从疾病目标研究、药物化合物筛选、临床试验服务、工艺研发、规模化生产

对于药物分析的工作人员来说,检验方法的验证和确认步骤是必须了解的知识。本文对检验方法的验证和确认步骤及详细计算方法进行整理,供各位同仁学习参考。一、检验方法验证的基本内容检验方法验证的基本内容包括方案的起草及审批,检测仪器的确认。适用性验证(包括准确度试验、精密度测定、线性范围试验

一、概述辅料一般被看作是惰性物质,但是当辅料被添加到制剂中时,某些辅料可能会对药物的最终药理学作用产生非常大的影响。药物和辅料之间的相互作用可能是物理化学作用,也可能是生理作用,对制剂的稳定性、安全性和有效性均有一定程度的影响。其相互作用大小与药物的性质、辅料的性质及其加入量均有较大的关系,其相互作
1、柱容量柱容量越大越不容易过载。决定柱容量的指标是柱截面上固定相的面积占比,它与空容、填料的比表面积、表面健合率等色谱参数有关。需要注意的是,增加柱长并不能增加柱容量,因为样品进样后不可能立即分布于整个色谱柱,同样因为无限直径效应的缘故,增大柱内径也不能增大柱容量。2、进样量显然,减小进样量可

作为学有机化学的,在平时工作实验中,最最不可缺少的就是TLC点板跟踪反应,而显色剂的种类大家都知道有多少种?好的显色剂不但能够让你工作更加效率,更多的有可能帮助你减少失误。那么今天,这一篇,笔者罗列了几乎所有常用的显色剂,希望能够帮助到大家。注:TLC在浸润以下显色剂后,都一般需要热烤才能显色!4-甲

薄层色谱(Thin-Layer Chromatography: TLC)是在玻璃板上,塑料片或者铝箔覆盖有很薄的一层吸附剂的一种用于分离混合物的色谱法。薄层板展开的方法是其中一端被溶剂浸润后,溶剂在吸附剂的间隙中扩散,溶剂往上方移动进行爬板(毛细管现象)。如果在板子上点样混合物的话,那么化合物也会随着溶剂的移动而移动。这个时候,

DMSO在酸性条件下,顶空加热至80℃以上易分解为甲硫醚、二甲基二硫醚和甲硫醇。建立盐酸盐类原料药的残留溶剂检测方法时,选用顶空进样方法测定时应避免使用二甲基亚砜(DMSO)做稀释剂,可选用水、N,N-二甲基甲酰胺等做稀释剂,可有效避免引入杂质峰干扰测定。◆DMSO在酸性条件下加热的反应机理方法建立背景我公司在
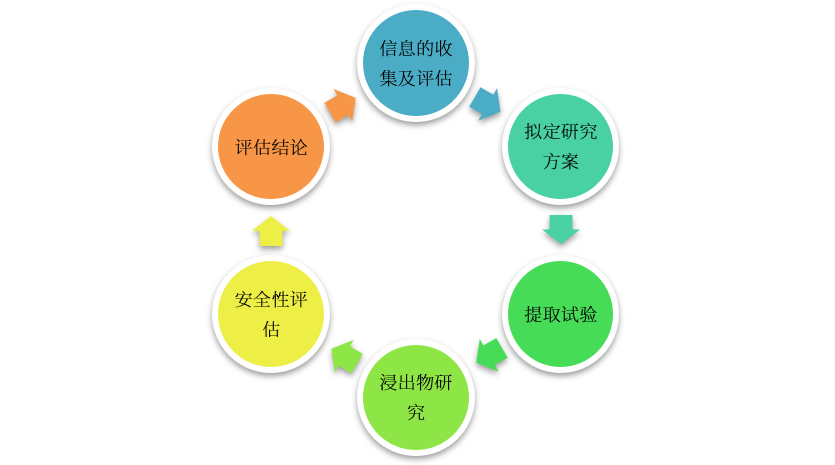
《化学药品注射剂仿制药质量和疗效一致性评价技术要求(征求意见稿)》[1]中明确提出注射剂需开展包装材料和容器的相容性研究。同时公众对药品的安全意识也在不断加强,对由包装系统引发的安全性问题关注度也日益增加,各国也出台了相应的法律法规及指导原则。《化学药物注射剂与塑料包装材料相容性研究技术指导原则(试行)》[

ICH Q7A 对于原料药(Active Pharmaceutical Ingredient, API)的定义:任何旨在供生产一种药物制剂,并作为其活性成分的物质或混合物,这类物质旨在疾病的诊断、治疗、缓减、处置和预防及影响人体的结构和功能等方面发挥药理作用或其他的直接效益。01原料药控制策略-有机杂质根据原料药的合成工艺
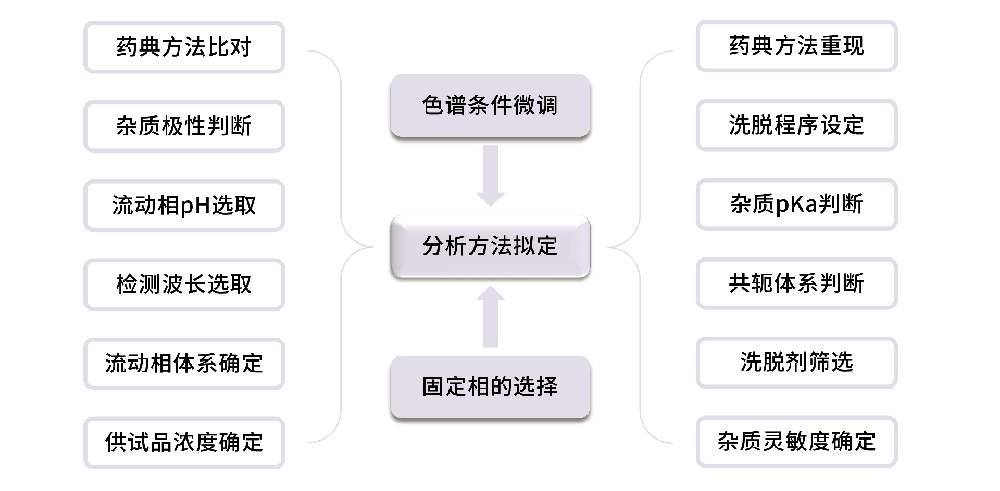
分析方法在药学质量研究中扮演重要的角色,普析手段目前还是在分析领域占据重要的位置,一般尤以HPLC-UV占比最大,一个好的分析方法能有效检出样品中存在的所有杂质,不遗漏某些杂质的检出,以免误导工艺人员正确的开发。 分析方法的建立往往在原
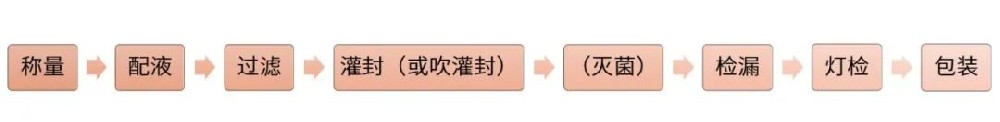
滴眼剂系指由原料药物与适宜辅料制成的供滴入眼内的无菌液体制剂,其生产和质量要求一般参考注射剂的技术要求。本文结合《化学药品注射剂仿制药质量和疗效一致性评价技术要求》等相关要求,具体阐述滴眼液研究过程中的研发内容及注意事项。参比制剂信息确认参比制剂来源确

根据国家相关法律法规要求,药品上市许可持有人(申请人)应当主动开展药品上市后研究,实现药品全生命周期管理。鼓励持有人运用新生产技术、新方法、新设备、新科技成果,不断改进和优化生产工艺,持续提高药品质量,提升药品安全性、有效性和质量可控性。但药品上市后变更不得对药品的安全性、有效性和质量可控性产生不良

为响应消费者对食品标签内容透明化的迫切需求,国家市场监督管理总局出台了《食品标识监督管理办法》(简称“《办法》”),并与国家卫生健康委员会联合发布新版《食品安全国家标准 预包装食品标签通则》(GB 7718-2025)(简称“GB 7718-2025”),进一步优化了预包装食品日期标识要求。此次修订结合市场监管经验及2011版标

2025年3月27日,随着《食品安全国家标准 预包装食品标签通则》(GB 7718-2025)的发布,我国正式将数字标签的相关要求纳入该标准,这标志着我国在食品标签数字化领域迈出了重要一步。与此同时,国际社会也在积极推进食品数字标签的标准化和规范化进程。例如,欧盟通过了多项法规,允许在葡萄酒、渔业和水产养殖产品等领域使

2025 年 3 月,中国发布了新版《食品安全国家标准 预包装食品营养标签通则》(GB 28050-2025),并将于2027年3月16日实施。这一标准的出台标志着中国在营养标签管理方面的重大变革。此次修订将强制标示的营养素从 “1+4”(能量、蛋白质、脂肪、碳水化合物、钠)扩展为 “1+6”,新增了糖和饱和脂肪(酸)两项内容。这

参考头孢地尼胶囊的说明书,每日最大用量为0.3g,根据FDA发布的《人用药中亚硝胺杂质控制》行业指南,NDMA和NDEA每日可接受摄入量分别为:96.0ng/天和26.5ng/天,计算N-亚硝基二甲胺(NDMA)限度为:96ng/day÷0.3g/day=320ppb,N-亚硝基二乙胺(NDEA)限度为:26.5ng/day÷0.3g/day=88ppb。根据上述限度要求,并参考《中国

1.酰胺类亚硝酸盐的致突变机制由上述致突变机制可知,普通亚硝胺类杂质通过CytP450酶作用,形成活性碳正离子,酰胺类主要通过重排形成。亚硝胺在体内产生毒性的作用机制(需代谢活化)与N-亚硝基脲(直接产生重氮化物或R自由基)不同,部分亚硝基化合物的毒性机制还没有确切结论,此外基于亚硝胺类化合物在药品

1. 核磁共振波谱仪:(1)送检样品纯度一般应>95% ,无铁屑、灰尘、滤纸毛等杂质。一般有机物须提供的样品量:1H谱>5mg,13C谱>15mg ,对聚合物所需的样品量应适当增加。(2)进行液体样品分析,要求样品在某种氘代溶剂中有良好的溶解性能,应先选好所用溶剂。常备的氘代溶剂有氯仿、重水、甲醇、丙酮、 DMSO 、苯

(一)个人防护装备的正确使用在实验室中,正确使用个人防护装备是保障自身安全的关键。常用防护装备包括手套、护目镜、口罩和防护服。手套需根据试剂特性选择,如接触DMSO或丙烯酰胺时,应佩戴防化学腐蚀的丁腈手套;护目镜可保护眼睛免受试剂飞溅伤害,如在混合强腐蚀性试剂TCA时,必须佩戴;口罩用于防止吸入有毒气体或粉

让我们深入了解这 17 种毒性试剂 ,以便在实验室操作中更好地保护自己和他人的安全。DMSO(二甲基亚砜):一种用途广泛的非质子极性溶剂,可溶解乙炔、芳烃、二氧化硫等气体,也常用于腈纶纤维纺丝。它能溶于水和有机溶剂,对皮肤有强渗透性,可用于药物透皮吸收和农药添加剂,还可作为细胞保护剂,降低细胞冰点,减少冰晶形